Estoy en Ciudad de México. Entro a un restaurant de comida típica. Leo el menú y me llama la atención el nombre de un platillo “Camarones a la diabla”. Pregunto si pica y me responden que no, no mucho. Luego del primer bocado lloro, toso, me ahogo. Mi vecino de mesa ríe y dice: te enchilaste. Superada la risa, pidió un vaso de leche y me lo ofreció. Alivio instantáneo. Años después, como químico viajero, entiendo que experimenté una batalla molecular entre capsaicina, receptores del dolor, y la química salvadora de las proteínas lácteas.
La molécula de fuego
La capsaicina (8-metil-N-vanillil-6-nonenamida) es el principal capsaicinoide responsable del picante en chiles del género Capsicum [1]. Su estructura molecular revela la clave: una cabeza aromática vanilloide polar conectada a una larga cola alifática hidrocarbonada [2]. Esta arquitectura bifásica determina todas sus propiedades.
Con fórmula C₁₈H₂₇NO₃ y peso molecular de 305.4 g/mol, la capsaicina es altamente lipofílica [3]. Su coeficiente de partición octanol-agua (log P ≈ 3.0-4.0) indica fuerte preferencia por ambientes grasos sobre acuosos [4]. Esta hidrofobicidad no es accidental: la capsaicina evolucionó para acumularse en membranas lipídicas, donde residen sus receptores objetivo [5].
La molécula presenta un grupo amida que forma puentes de hidrógeno, un anillo aromático con grupos hidroxilo y metoxilo para interacciones π-π, y una cadena hidrocarbonada que se inserta en bicapas lipídicas [6]. Esta combinación permite atravesar membranas y alcanzar sitios de unión específicos [7].

El Engaño Molecular: Receptores TRPV1
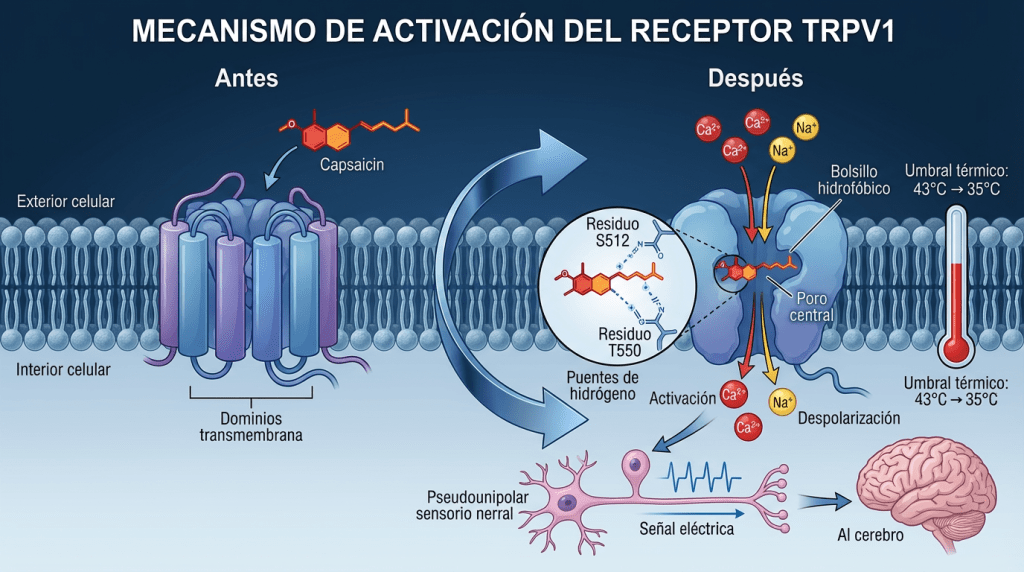
El ardor del picante no es sabor, sino dolor. La capsaicina activa el receptor TRPV1 (Transient Receptor Potential Vanilloid 1), un canal iónico que normalmente detecta calor nocivo (>43°C) [8]. Este receptor en neuronas sensoriales es nuestro sistema de alarma contra quemaduras [9].
A nivel molecular, la capsaicina se une a un bolsillo hidrofóbico en el dominio transmembrana del TRPV1 [10]. Estudios cristalográficos revelan que la cabeza vanilloide forma puentes de hidrógeno con residuos de serina (S512) y treonina (T550), mientras su cola hidrocarbonada se inserta entre hélices transmembrana S3 y S4, estabilizándose mediante interacciones de van der Waals [11], [12].
Esta unión induce un cambio conformacional que abre el canal, permitiendo entrada masiva de iones calcio y sodio [13]. El influjo iónico despolariza la neurona, generando potenciales de acción que el cerebro interpreta como “calor doloroso” [14]. El engaño es perfecto: capsaicina a temperatura ambiente activa los mismos circuitos que una quemadura real [15].
La sensibilidad del TRPV1 es extraordinaria: concentraciones nanomolares (10⁻⁹ M) son suficientes para activarlo [16]. Esta alta afinidad explica por qué cantidades minúsculas producen sensaciones intensas [17].
Por Qué el Agua No Funciona
Mi error en Bangkok tiene explicación molecular clara. La capsaicina es extremadamente hidrofóbica: su solubilidad en agua es menor a 10 mg/L a 25°C [18]. Cuando bebemos agua tras comer picante, la capsaicina ya está unida a receptores TRPV1 en membranas lipídicas de la mucosa oral [19].
El agua no puede disolver ni remover capsaicina de estos sitios hidrofóbicos. Peor aún, simplemente redistribuye moléculas no unidas por toda la cavidad oral, expandiendo el área de contacto y aumentando el ardor [20]. Es como intentar limpiar aceite con agua: las moléculas se repelen por incompatibilidad entre compuestos polares (agua) y apolares (capsaicina) [21].
La regla química “lo similar disuelve lo similar” es implacable: necesitamos un solvente lipofílico o un agente que secuestre la capsaicina [22].
El Antídoto Lácteo: Caseína al Rescate
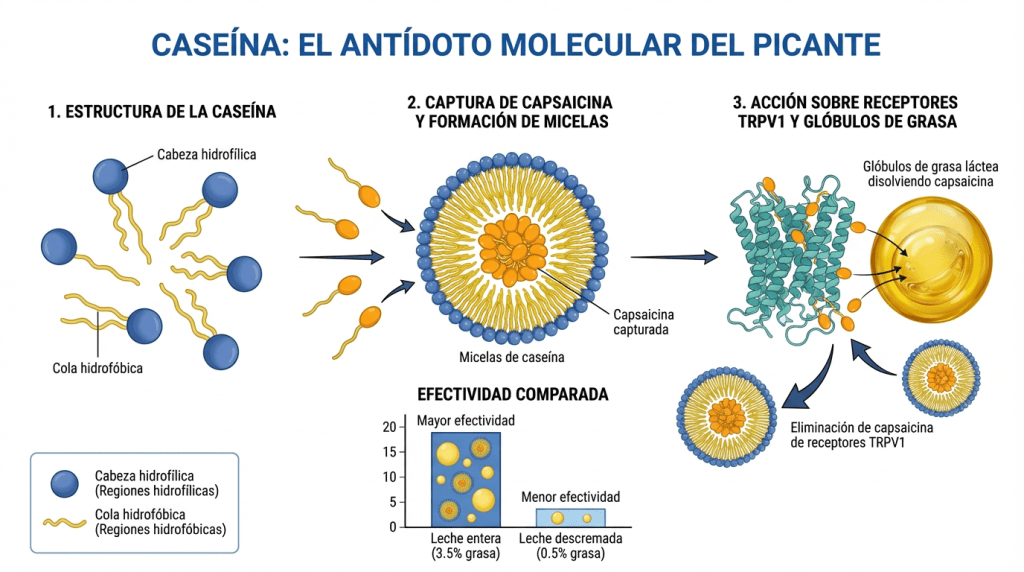
La leche funciona por una razón bioquímica elegante: la caseína, su principal proteína (~80% de proteínas lácteas), actúa como detergente molecular [23]. La caseína es una fosfoproteína anfipática con regiones hidrofóbicas e hidrofílicas [24].
Estudios de espectroscopía demuestran que la caseína se une a capsaicina mediante interacciones hidrofóbicas [25]. Las regiones hidrofóbicas de la caseína envuelven la cola apolar de la capsaicina, formando complejos micelares que solubilizan la molécula picante [26].
Este “secuestro molecular” tiene dos efectos: primero, la caseína compite con TRPV1 por la capsaicina, reduciendo la cantidad disponible para activar receptores [27]; segundo, los complejos caseína-capsaicina son solubles en saliva y pueden tragarse, removiendo físicamente el irritante [28].
La grasa láctea (3-4% en leche entera) también contribuye, disolviendo directamente capsaicina por afinidad lipídica [29]. Por eso la leche entera es más efectiva que la descremada, y productos como yogur o helado son antídotos excelentes [30].
La Escala Scoville
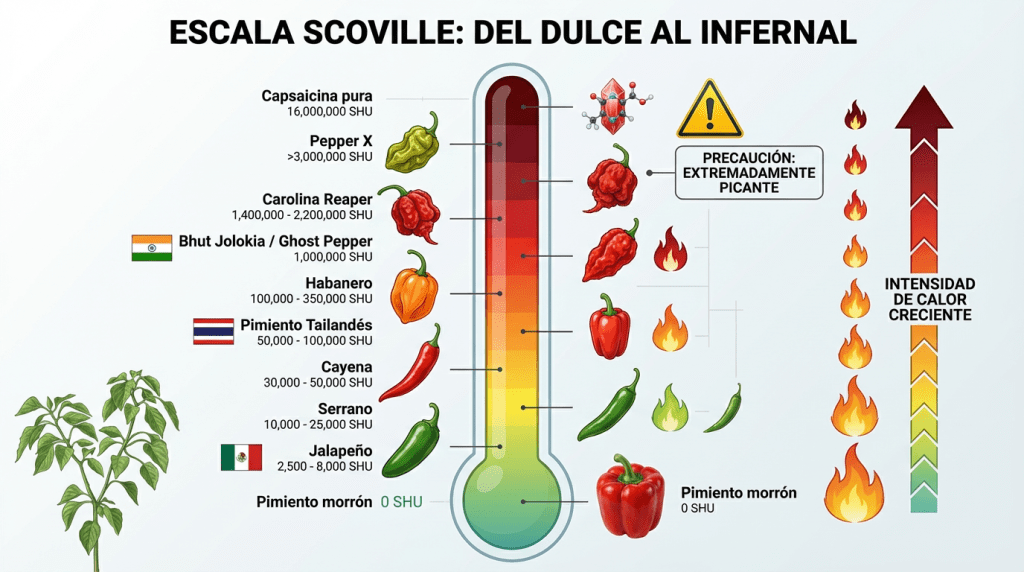
La escala Scoville, desarrollada en 1912 por el farmacéutico Wilbur Scoville, cuantifica el picante mediante Unidades de Calor Scoville (SHU) [1]. Originalmente, extractos de chile se diluían en agua azucarada hasta que el picante dejaba de detectarse [26]. Un pimiento que requería dilución 1:1000 tenía 1000 SHU. Hoy, cromatografía líquida (HPLC) mide directamente la concentración de capsaicinoides, convirtiendo partes por millón a SHU mediante: SHU = ppm de capsaicina × 15-16 [26]. Las diferencias reflejan variaciones genéticas en biosíntesis de capsaicinoides, moduladas por temperatura, estrés hídrico y disponibilidad de nitrógeno [16].
Conclusiones: Cada experiencia con picante es un experimento bioquímico: moléculas hidrofóbicas engañando receptores térmicos, proteínas lácteas como rescatistas moleculares, y nuestro cerebro interpretando señales químicas como calor y dolor. La próxima vez que enfrentes un chile habanero en Yucatán o un curry vindaloo en Goa, recuerda: es química pura. Y por favor, olvida el agua. Pide leche.
Referencias
[1] T. Suzuki, K. Iwai, “Constituents of Red Pepper Species: Chemistry, Biochemistry, Pharmacology, and Food Science of the Pungent Principle of Capsicum Species,” The Alkaloids: Chemistry and Pharmacology, vol. 23, pp. 227-299, 1984.
[2] S. Conway, “TRPing the switch on pain: an introduction to the chemistry and biology of capsaicin and TRPV1,” Chemical Society Reviews, vol. 37, no. 8, pp. 1530-1545, 2008.
[3] G. Appendino, “Capsaicin and capsaicinoids,” in Bioactive Compounds from Natural Sources, 2nd ed., CRC Press, 2007, ch. 4.
[4] S. Basith, B. Cui, W. Hong, S. Choi, “Harnessing the Therapeutic Potential of Capsaicin and Its Analogues in Pain and Other Diseases,” Molecules, vol. 21, no. 8, p. 966, 2016.
[5] S. M. Hanson et al., “Capsaicin interaction with TRPV1 channels in a lipid bilayer: molecular dynamics simulation,” Biophysical Journal, vol. 108, no. 6, pp. 1425-1434, 2015.
[6] F. Yang et al., “Structural mechanism underlying capsaicin binding and activation of the TRPV1 ion channel,” Nature Chemical Biology, vol. 11, no. 7, pp. 518-524, 2015.
[7] L. Darré, I. Domene, “Binding of Capsaicin to the TRPV1 Ion Channel,” Molecular Pharmaceutics, vol. 12, no. 12, pp. 4454-4465, 2015.
[8] F. Yang, J. Zheng, “Understand spiciness: mechanism of TRPV1 channel activation by capsaicin,” Protein & Cell, vol. 8, no. 3, pp. 169-177, 2017.
[9] D. N. Cortright, A. Szallasi, “Biochemical pharmacology of the vanilloid receptor TRPV1: an update,” European Journal of Biochemistry, vol. 271, no. 10, pp. 1814-1819, 2004.
[10] K. M. Elokely et al., “Understanding TRPV1 activation by ligands: Insights from the binding modes of capsaicin and resiniferatoxin,” Proceedings of the National Academy of Sciences, vol. 113, no. 2, pp. E137-E145, 2016.
[11] F. Yang et al., “Molecular Mechanism of TRPV1 Activation by Capsaicin,” Biophysical Journal, vol. 108, no. 2, p. 406a, 2015.
[12] Z. Sun et al., “Mechanism of capsaicin entry into buried vanilloid sites in TRPV1,” Nature Chemical Biology, vol. 21, pp. 234-243, 2025.
[13] L. Amaya-Rodriguez et al., “A journey from molecule to physiology and in silico tools for drug discovery targeting the transient receptor potential vanilloid type 1 (TRPV1) channel,” Frontiers in Pharmacology, vol. 14, p. 1251061, 2024.
[14] S. Rusterholz, “Capsaicin, from Hot to Not; Can New Pain-Relieving Drugs Be Derived from This Substance Known to Cause Pain?,” Journal of Chemical Education, vol. 83, no. 12, p. 1809, 2006.
[15] R. Sinha et al., “Capsaicin: Unveiling its Therapeutic Potential and Pharmacological Actions,” Current Bioactive Compounds, 2024.
[16] I. Guzman et al., “A Matter of Taste: Capsaicinoid Diversity in Chile Peppers and the Importance to Human Food Preference,” in Capsicum – Current Trends and Perspectives, IntechOpen, 2018.
[17] J. A. Caballero, “A new era for the design of TRPV1 antagonists and agonists with the use of structural information and molecular docking of capsaicin-like compounds,” Journal of Enzyme Inhibition and Medicinal Chemistry, vol. 37, no. 1, pp. 2166-2180, 2022.
[18] M. A. Razzak et al., “Molecular characterization of capsaicin binding interactions with ovalbumin and casein,” Food Hydrocolloids, vol. 132, p. 107991, 2022.
[19] S. Basharat et al., “Capsaicin: Plants of the Genus Capsicum and Positive Effect of Oriental Spice on Skin Health,” Skin Pharmacology and Physiology, vol. 34, no. 1, pp. 8-19, 2021.
[20] Y. Wahyuni, “Breeding for pepper fruit quality: a genetical metabolomics approach,” Ph.D. dissertation, Wageningen University, Netherlands, 2014.
[21] C. M. T. Pinto et al., “Pimenta capsicum: propriedades químicas, nutricionais, farmacológicas e medicinais e seu potencial para o agronegócio,” Revista Brasileira de Agropecuária Sustentável, vol. 3, no. 2, pp. 108-120, 2013.
[22] G. Appendino et al., “Capsaicin and capsaicinoids,” in Bioactive Compounds from Natural Sources, 2nd ed., CRC Press, 2007.
[23] Z. Farah, “The effect of interactions between capsaicin and dairy proteins on oral burn,” Ph.D. dissertation, University of Guelph, Canada.
[24] M. A. Razzak et al., “Molecular characterization of capsaicin binding interactions with ovalbumin and casein,” Food Hydrocolloids, vol. 132, p. 107991, 2022.
[25] M. A. Razzak et al., “Molecular characterization of capsaicin binding interactions with ovalbumin and casein,” Food Hydrocolloids, vol. 132, p. 107991, 2022.
[26] P. W. Bosland et al., “‘Trinidad Moruga Scorpion’ Pepper is the World’s Hottest Measured Chile Pepper at More Than Two Million Scoville Heat Units,” HortTechnology, vol. 22, no. 4, pp. 534-538, 2012.
[27] Z. Farah, “The effect of interactions between capsaicin and dairy proteins on oral burn,” Ph.D. dissertation, University of Guelph, Canada.
[28] M. A. Razzak et al., “Molecular characterization of capsaicin binding interactions with ovalbumin and casein,” Food Hydrocolloids, vol. 132, p. 107991, 2022.
[29] S. Basharat et al., “Capsaicin: Plants of the Genus Capsicum and Positive Effect of Oriental Spice on Skin Health,” Skin Pharmacology and Physiology, vol. 34, no. 1, pp. 8-19, 2021.
[30] M. A. Razzak et al., “Molecular characterization of capsaicin binding interactions with ovalbumin and casein,” Food Hydrocolloids, vol. 132, p. 107991, 2022.